炭酸ナトリウム106gに塩酸を加えていくと、重そう(炭 酸水素ナトリウム)84gと食塩58.5gができます。すべての炭酸ナトリウムが重そうに変わったのち、さらに塩酸を加えていくと、 重そうと塩酸が反応し、二酸化炭素22.4L(44g)が発生して水18gと食塩58.5gができます。
また水酸化ナトリウム80gは塩化水素73gと反応し水36gと食塩ができます。
今、炭酸ナトリウムと水酸化ナトリウムの混合物に塩酸を加えていき、加えた塩酸の重さと発生した二酸化炭素の体積の関係を調べると下 の図のようになりました。
混合物にふくまれていた炭酸ナトリウムと水酸化ナトリウムの重さをそれぞれ求めなさい。
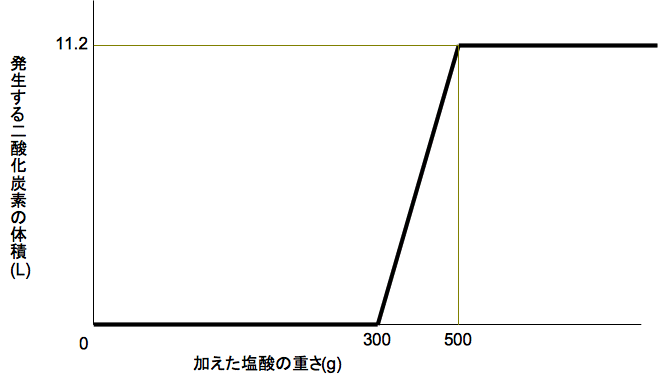
加えた塩酸が300gまでの間は、炭酸ナトリウムが重そうに変わりながら、水酸化ナトリウムが塩酸で中和されている。
加え た塩酸が300g〜500gまでの間では、重そうが塩酸と反応して二酸化炭素が発生している。
つまり、二酸化炭素→重そう→炭酸ナトリウムの順に逆戻しで重さを求めていけばよい。
重そう + 塩化水素→水 + 二酸化炭素 + 食塩
84g 36.5g 18g 44g(22.4L) 58.5g
二酸化炭素が0.5倍になっているので、他も0.5倍して
42g 18.25g 9g 22g(11.2L) 29.25g
炭酸ナトリウム + 塩化水素 → 重そう + 食塩
106g 36.5g 84g 58.5g
重そう42gで0.5倍になっているので、他も0.5倍して
53g 18.25g 42g 29.25g
またグラフより塩酸200gが重そうと反応しており、このとき塩化水素18.25gとなったので、塩酸100g中では塩化水 素が9.125gとけているはず。
炭酸ナトリウムを重そうに変えるときも同量の塩化水素が使われているので、水酸化ナトリウムと反応した塩酸は 300g−200g=100gである。
すなわち、
水酸化ナトリウム + 塩化水素 → 水 + 食塩
80g 73g 36g 117g
塩化水素が9.125÷73g=0.125倍になっているので、他も0.125倍して
10g 9.125g 14.625g
答え 炭酸ナトリウム53g、水酸化ナトリウム10g